Palladium(II)-bromid
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
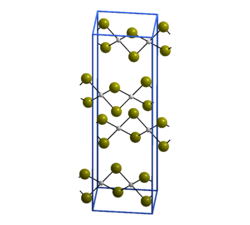
| Kristallstruktur von Palladium(II)-bromid _ Pd2+ _ Br− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Palladium(II)-bromid | |||||||||||||||
| Andere Namen |
Palladiumdibromid | |||||||||||||||
| Verhältnisformel | PdBr2 | |||||||||||||||
| Kurzbeschreibung |
schwarzer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 266,22 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
5,35 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Palladium(II)-bromid ist eine anorganische chemische Verbindung des Palladiums aus der Gruppe der Bromide.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Palladium(II)-bromid kann durch Reaktion von Palladium mit einer Bromwasserstoff-Brom-Lösung gewonnen werden.[3] Es kann auch direkt aus den Elementen gewonnen werden.[4]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Palladium(II)-bromid ist ein braunschwarzer Feststoff, der in Form von nadelförmigen Kristallen vorliegt. Er ist unlöslich in Wasser und organischen Lösungsmitteln, aber löslich in Halogenwasserstoffsäuren.[3] Er kristallisiert monoklin in der Raumgruppe P21/c (Raumgruppen-Nr. 14) mit den Gitterparametern a = 659 pm, b = 396 pm, c = 2522 pm und β = 92,6° sowie vier Formeleinheiten pro Elementarzelle.[2] Im Kristall ist jedes Palladiumatom quadratisch-planar von vier Bromatomen umgeben, jedes Bromatom bindet dabei an ein weiteres Palladiumatom, so dass unendliche Zickzackketten entstehen.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Palladium(II)-bromid kann als Katalysator in der organischen Chemie verwendet werden, wobei es teilweise aktiver ist als Palladium(II)-chlorid.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Datenblatt Palladium(II) bromide, Premion®, 99.998% (metals basis), Pd 39.5% min bei Alfa Aesar, abgerufen am 30. August 2013 (Seite nicht mehr abrufbar).
- ↑ a b c d Jean d’Ans, Ellen Lax, Roger Blachnik: Taschenbuch für Chemiker und Physiker. Springer, 1998, ISBN 3-642-58842-5, S. 668 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1730.
- ↑ Catherine E. Housecroft: Inorganic Chemistry. Pearson Education, 2005, ISBN 0-13-039913-2, S. 686 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Jiro Tsuji: Palladium Reagents and Catalysts: New Perspectives for the 21st Century. John Wiley & Sons, 2006, ISBN 0-470-02119-5, S. 344 (eingeschränkte Vorschau in der Google-Buchsuche).
