Atherton-Todd-Reaktion
Die Atherton-Todd-Reaktion ist eine Namensreaktion der organischen Chemie, die auf die britischen Chemiker F. R. Atherton, H. T. Openshaw und A. R. Todd zurückgeht. Diese beschrieben die Reaktion erstmals 1945 als Methode zur Umwandlung von Dialkylphosphiten in Dialkylchlorphosphate.[1] Die gebildeten Dialkylchlorphosphate sind häufig zu reaktiv, um isoliert zu werden. Aus diesem Grund kann sich bei Anwesenheit von Alkoholen oder Aminen die Synthese von Phosphaten oder Phosphoramidaten an die Atherton-Todd-Reaktion anschließen.
Übersichtsreaktion
[Bearbeiten | Quelltext bearbeiten]Die folgende Reaktionsgleichung gibt eine Übersicht für die Atherton-Todd-Reaktion anhand des Beispiels Dimethylphosphit als Reaktant:
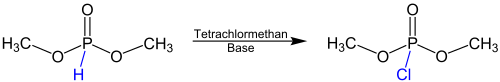
Die Reaktion erfolgt unter Zugabe von Tetrachlormethan und einer Base. Bei dieser Base handelt es sich üblicherweise um ein primäres, sekundäres oder tertiäres Amin. Anstelle der Methylgruppen können auch andere Alkylgruppen oder Benzylgruppen vorliegen.
Reaktionsmechanismus
[Bearbeiten | Quelltext bearbeiten]Ein möglicher Reaktionsmechanismus für die Atherton-Todd-Reaktion soll entsprechend der Übersichtsreaktion am Beispiel der Ausgangsverbindung Dimethylphosphit erläutert werden:[2]

Zunächst wird ein tertiäres Amin verwendet, um eine Methylgruppe des Dimethylphosphits abzuspalten. Aus diesem Reaktionsschritt geht die Zwischenstufe 1 hervor.

Anschließend folgt die Protonierung der Zwischenstufe 1 durch die Ausgangsverbindung Dimethylphosphit. Diese wird im Gegenzug deprotoniert, so dass Zwischenstufe 2a und Zwischenstufe 2b gebildet werden. Dann wird aus der Zwischenstufe 2a die Zwischenstufe 1 zurückgewonnen.

Schließlich wird die Zwischenstufe 2b mittels Tetrachlormethan chloriert und es entsteht Dimethylchlorphosphat 3.
Möglicher weiterer Reaktionsverlauf
[Bearbeiten | Quelltext bearbeiten]Nach der Synthese des Dimethylchlorphosphats ist eine Weiterreaktion, beispielsweise mit einem primären Amin (z. B. Anilin), nach der folgenden Reaktionsgleichung möglich:[3]

Atomökonomie
[Bearbeiten | Quelltext bearbeiten]Bei dieser Reaktion werden neben dem Dialkylphosphit als Ausgangsverbindung Tetrachlormethan in stöchiometrischer Menge und eine Base (Amin) eingesetzt. Gleichzeitig wird die Ausgangsverbindung selbst als Reagenz verwendet, allerdings nicht in stöchiometrischer Menge. Somit ist lediglich Chloroform, das nach zwei Reaktionsschritten aus Tetrachlormethan hervorgeht, als Abfallprodukt für die Beurteilung der Atomökonomie relevant. Außerdem ist zu bedenken, dass das Produkt der Reaktion eine größere molare Masse als die Ausgangsverbindung aufweist. Die Atomökonomie dieser Reaktion ist demzufolge als relativ gut einzustufen.
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Die Atherton-Todd-Reaktion ist verwandt mit der Appel-Reaktion. Auch hier wird Tetrachlormethan zur Chlorierung genutzt.[2]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ F. R. Atherton, H. T. Openshaw, A. R. Todd: 174. Studies on phosphorylation. Part II. The reaction of dialkyl phosphites with polyhalogen compounds in presence of bases. A new method for the phosphorylation of amines. In: Journal of the Chemical Society (Resumed). 1945, S. 660–663, doi:10.1039/jr9450000660.
- ↑ a b Zerong Wang: Comprehensive organic name reactions and reagents Volume 1. John Wiley, Hoboken (N.J.) 2009, ISBN 978-0-470-28662-3, S. 114–118.
- ↑ Stéphanie S. Le Corre, Mathieu Berchel, Hélène Couthon-Gourvès, Jean-Pierre Haelters, Paul-Alain Jaffrès: Atherton–Todd reaction: mechanism, scope and applications. In: Beilstein Journal of Organic Chemistry. Band 10, Nr. 1, 2014, S. 1166–1196, doi:10.3762/bjoc.10.117.